Przykład 5.
Cząsteczka amoniaku
Cząsteczka amoniaku jest zbudowana z 1 atomu azotu i 3 atomów wodoru.
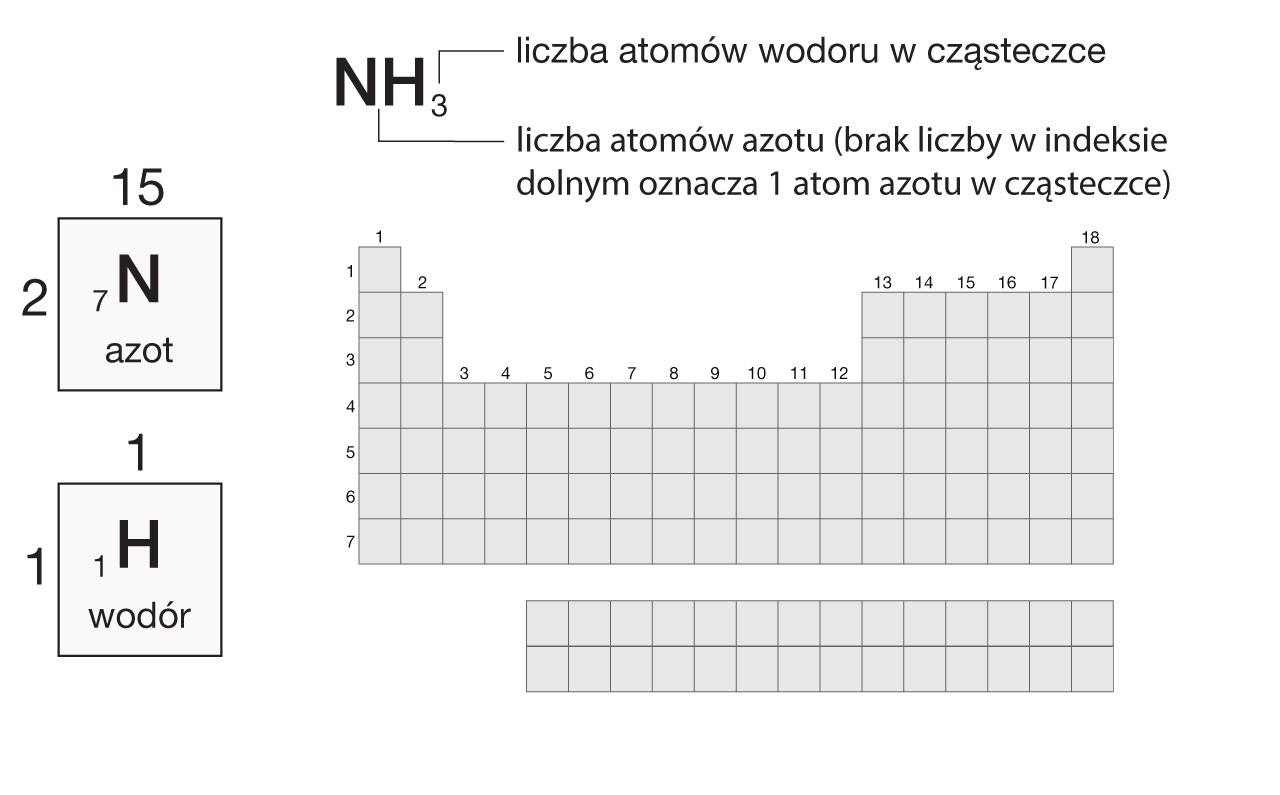
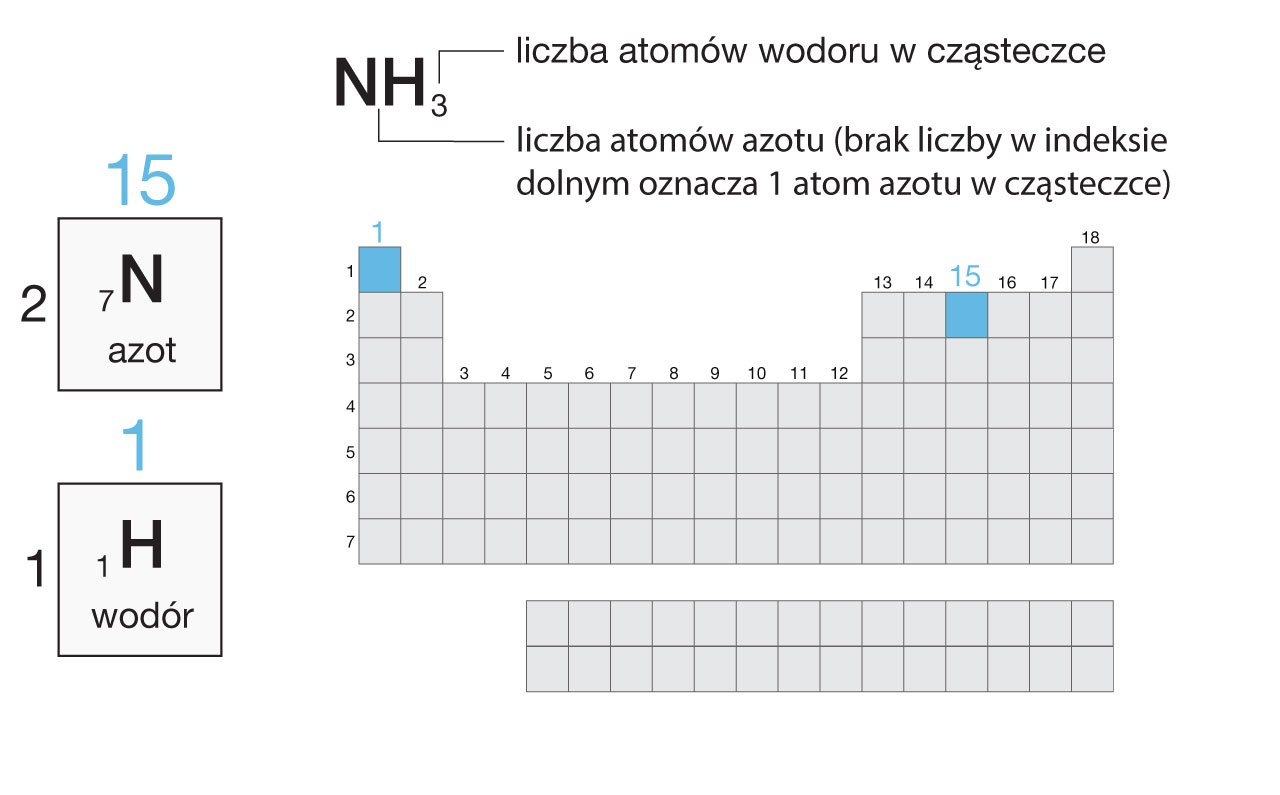
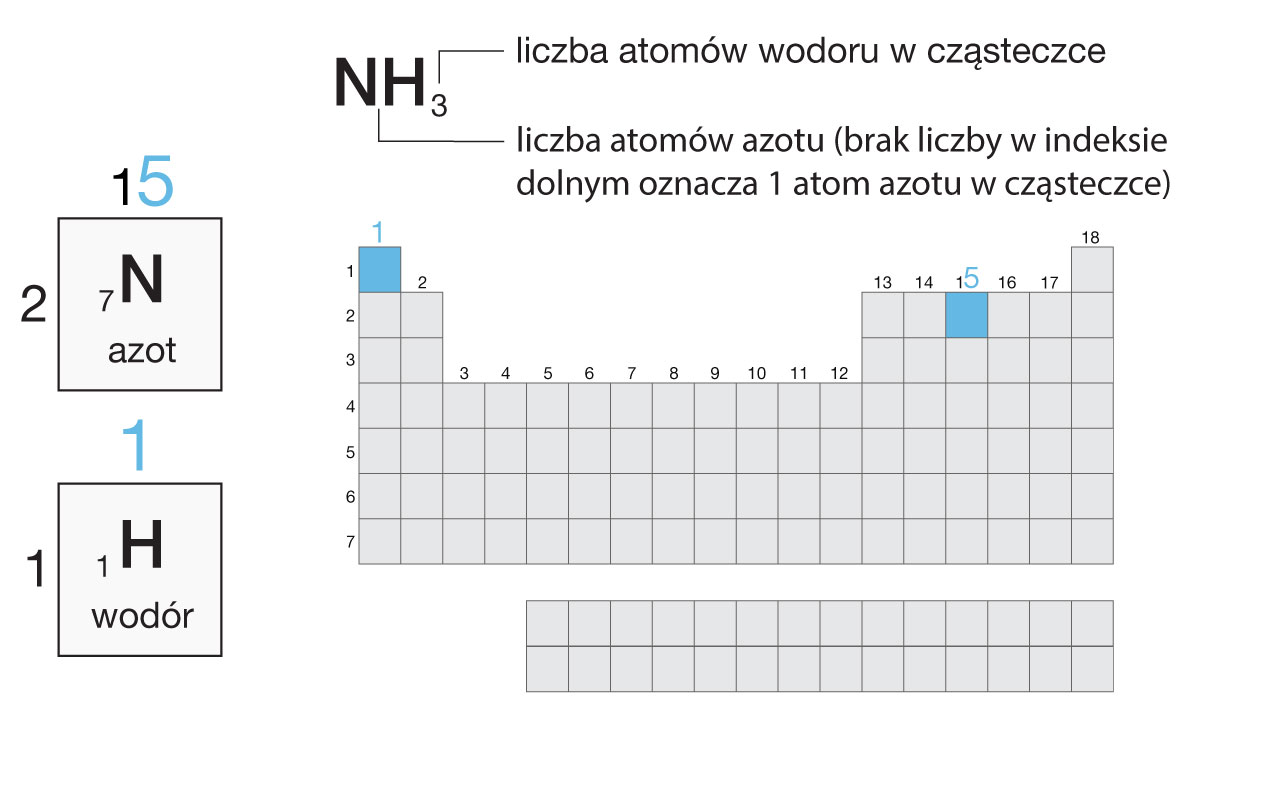
Azot znajduje się w grupie 15., czyli atom azotu ma 5 elektronów walencyjnych.
Wodór – w grupie 1. Atom wodoru ma więc 1 elektron walencyjny.
numer grupy układu okresowego
liczba elektronów walencyjnych
dla grup 1. i 2.
liczba elektronów walencyjnych = numer grupy
liczba elektronów walencyjnych atomu wodoru = 1
dla grup 13.–18.
liczba elektronów walencyjnych = numer grupy – 10
liczba elektronów walencyjnych atomu azotu = 5
- Ilu elektronów brakuje atomowi azotu, aby mógł uzyskać oktet elektronowy?
1 elektronu
3 elektronów
 Oktet elektronowy to 8 elektronów walencyjnych. Atom azotu ma 5 elektronów walencyjnych, więc potrzebuje jeszcze 3 elektronów do uzyskania oktetu.
Oktet elektronowy to 8 elektronów walencyjnych. Atom azotu ma 5 elektronów walencyjnych, więc potrzebuje jeszcze 3 elektronów do uzyskania oktetu. Atom azotu ma 5 elektronów walencyjnych, więc potrzebuje jeszcze 3 elektronów do uzyskania oktetu.
Atom azotu ma 5 elektronów walencyjnych, więc potrzebuje jeszcze 3 elektronów do uzyskania oktetu. - Ilu elektronów brakuje atomowi wodoru, aby mógł uzyskać dublet elektronowy?
1 elektronu
2 elektronów
 Atom wodoru ma 1 elektron walencyjny, więc potrzebuje jeszcze 1 elektronu do uzyskania dubletu.
Atom wodoru ma 1 elektron walencyjny, więc potrzebuje jeszcze 1 elektronu do uzyskania dubletu. Dublet elektronowy to 2 elektrony walencyjne. Atom wodoru ma 1 elektron walencyjny, więc potrzebuje jeszcze 1 elektronu do dubletu.
Dublet elektronowy to 2 elektrony walencyjne. Atom wodoru ma 1 elektron walencyjny, więc potrzebuje jeszcze 1 elektronu do dubletu. - Ile wspólnych par elektronowych musi wytworzyć się między atomem azotu i atomami wodoru, aby atomy uzyskały trwały stan elektronowy?
1 wspólna para elektronowa
3 wspólne pary elektronowe
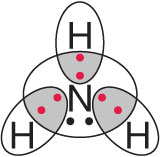 Atom azotu potrzebuje 3 elektronów, aby powstał oktet, a każdy z 3 atomów wodoru – 1 elektronu do dubletu, dlatego wytworzą się 3 wspólne pary elektronowe.
Atom azotu potrzebuje 3 elektronów, aby powstał oktet, a każdy z 3 atomów wodoru – 1 elektronu do dubletu, dlatego wytworzą się 3 wspólne pary elektronowe. Atom azotu potrzebuje 3 elektronów, aby powstał oktet, a każdy z 3 atomów wodoru – 1 elektronu do dubletu, dlatego wytworzą się 3 wspólne pary elektronowe.
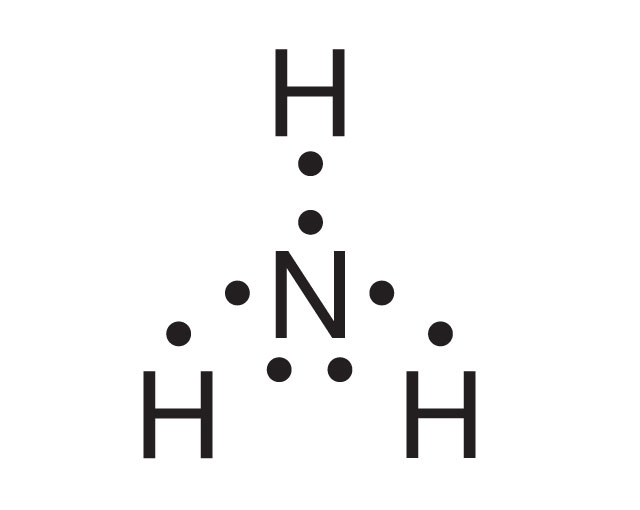
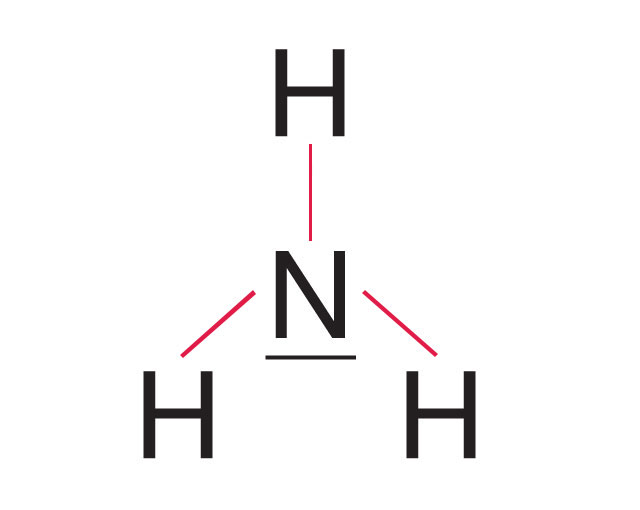
Atom azotu potrzebuje 3 elektronów, aby powstał oktet, a każdy z 3 atomów wodoru – 1 elektronu do dubletu, dlatego wytworzą się 3 wspólne pary elektronowe. - Schemat powstawania wiązania w cząsteczce amoniaku
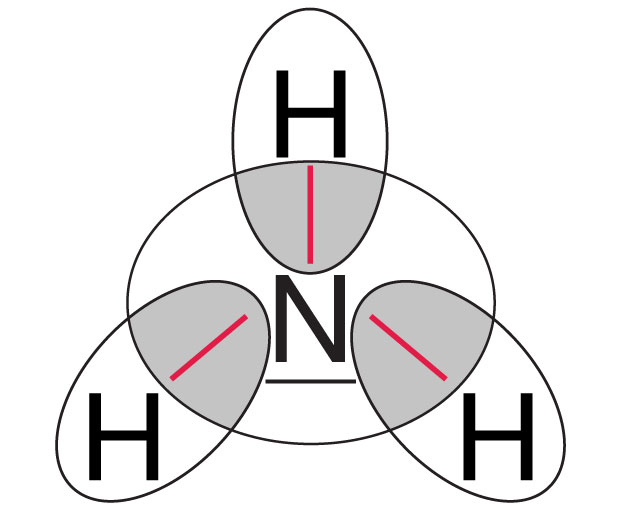
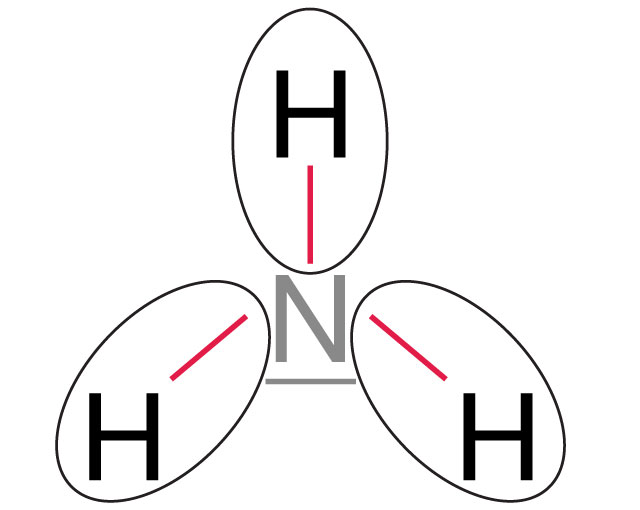
Uwspólnione elektrony
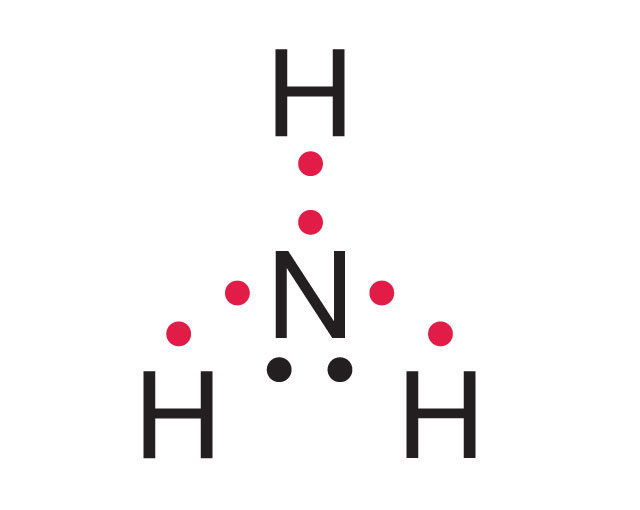
Wspólne pary elektronowe
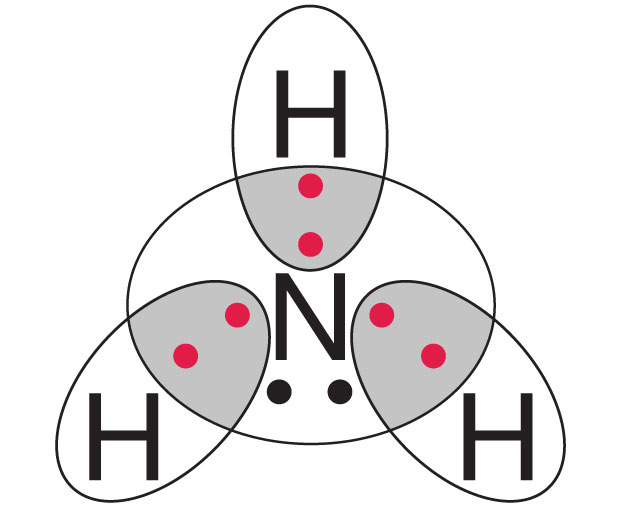
Elektrony tworzące oktet elektronowy lub dublet elektronowy
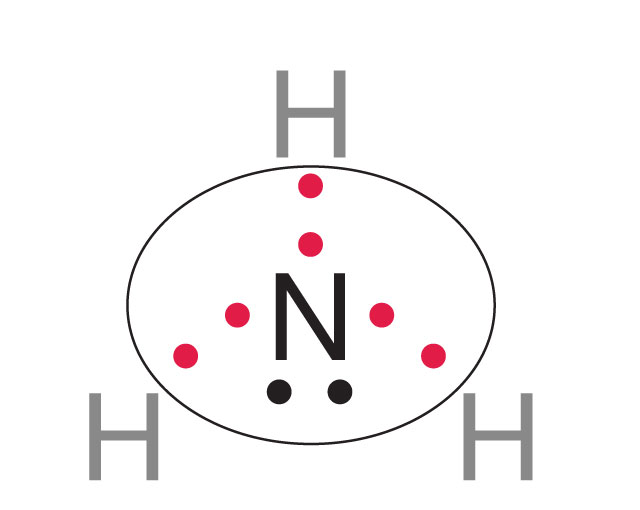
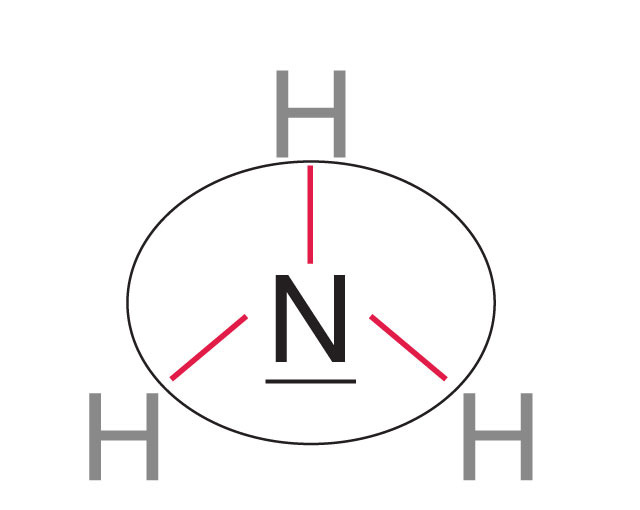
Polaryzacja wspólnych par elektronowych
Wzór strukturalny
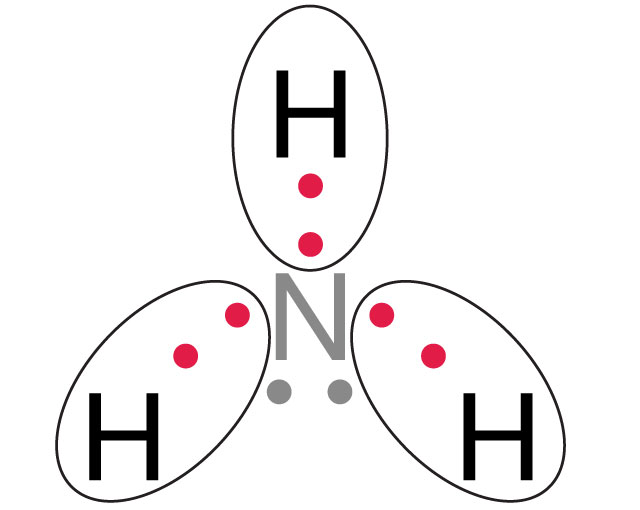
Liczba par elektronowych:
- w cząsteczce: 6e– tworzy 3 wspólne pary elektronowe
- w atomie azotu: 2e– tworzą 1 wolną parę elektronową
Oznaczenia elektronów:
• elektrony tworzące wspólne pary elektronowe
• elektrony tworzące wolną parę elektronową
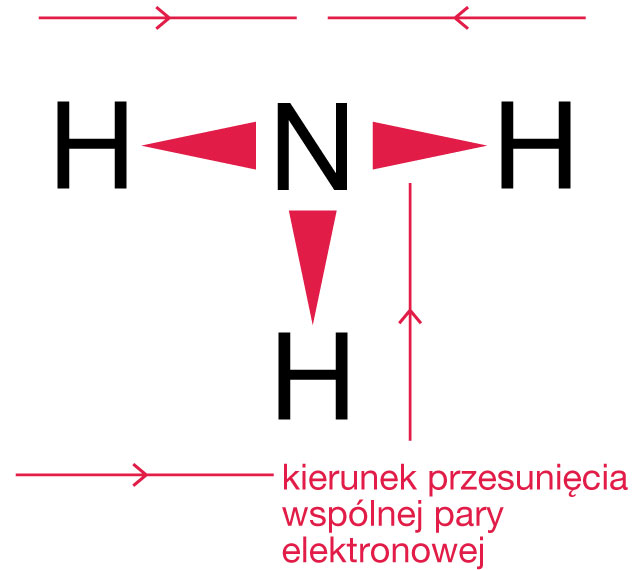
W wiązaniu kowalencyjnym spolaryzowanym wspólne pary elektronowe są przesunięte w stronę jednego z atomów o większej liczbie elektronów walencyjnych.
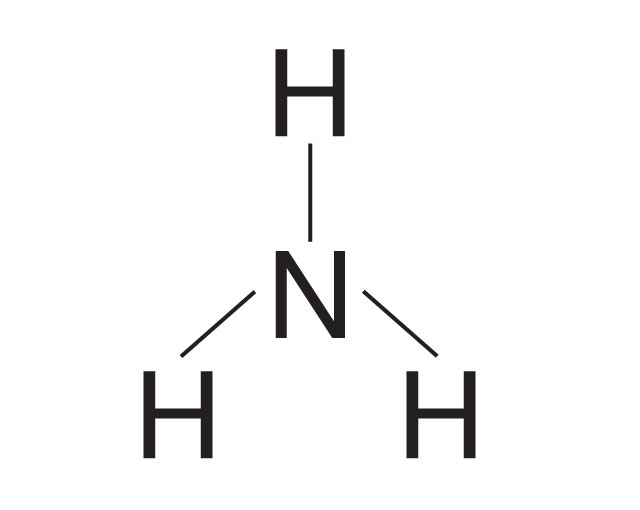
Uwspólnione elektrony
Wspólne pary elektronowe
Elektrony tworzące oktet elektronowy lub dublet elektronowy
Polaryzacja wspólnych par elektronowych
Wzór strukturalny
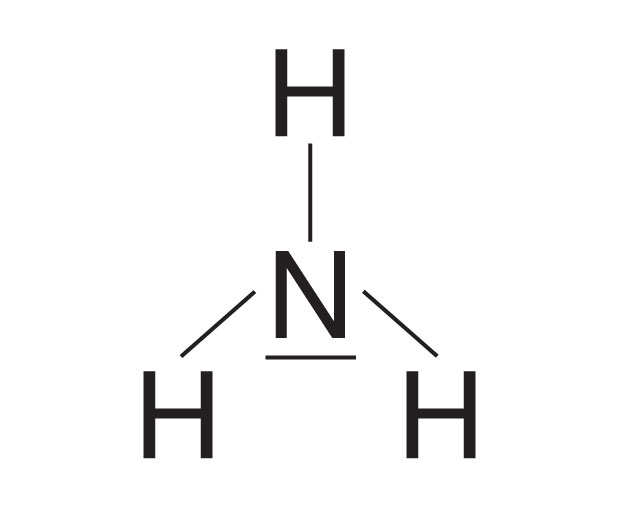
Liczba par elektronowych:
- w cząsteczce: 6e– tworzy 3 wspólne pary elektronowe
- w atomie azotu: 2e– tworzą 1 wolną parę elektronową
Oznaczenia elektronów:
— wspólna para elektronowa
— wolna para elektronowa

W wiązaniu kowalencyjnym spolaryzowanym wspólne pary elektronowe są przesunięte w stronę jednego z atomów o większej liczbie elektronów walencyjnych.

- Powstawanie wiązania kowalencyjnego spolaryzowanego – symulacja